Résumé
- Les chercheurs ont traité la drépanocytose chez la souris en modifiant directement le gène défectueux de l’hémoglobine qui cause cette maladie.
- Ces résultats pourraient conduire à un traitement ponctuel de la drépanocytose avec moins d’effets secondaires que les autres méthodes de traitement en cours de développement.
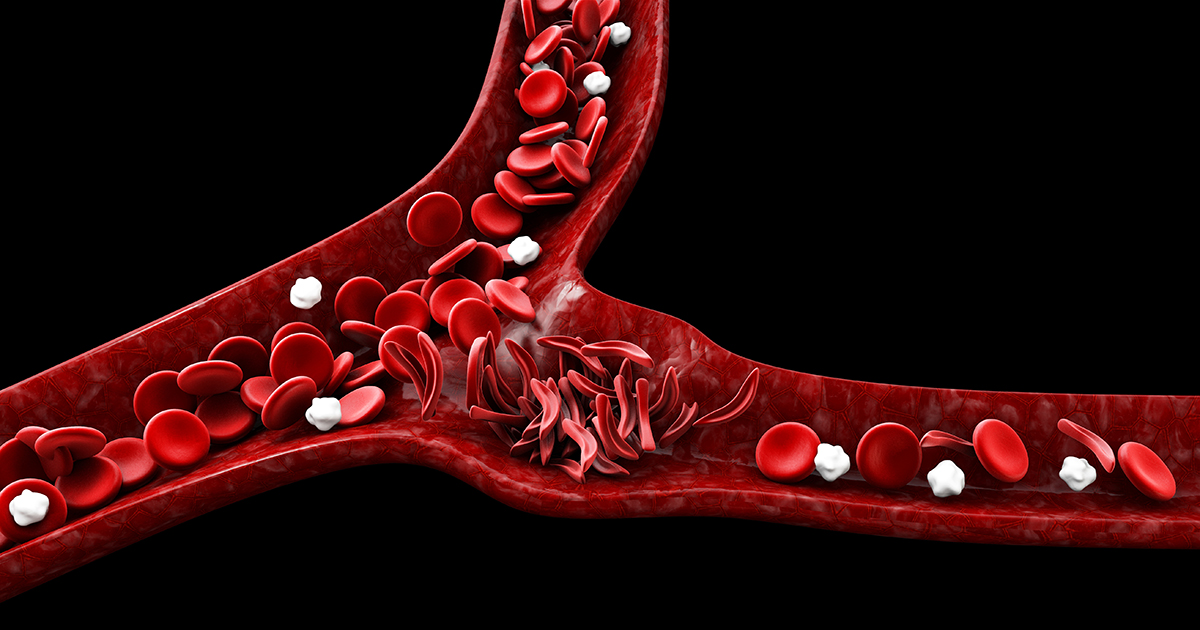
La drépanocytose (SCD) est une maladie génétique causée par une mutation dans les deux copies du gène HBB d’une personne. Ce gène code pour un composant de l’hémoglobine, qui est la protéine transportant l’oxygène dans les globules rouges. La mutation provoque le collage des molécules d’hémoglobine, créant des globules rouges en forme de faucille. Ce processus peut entraîner une rupture des cellules sanguines, une anémie, des douleurs récurrentes, une immunodéficience, des dommages aux organes et une mort prématurée. Les greffes de moelle osseuse peuvent guérir la drépanocytose, mais il est difficile de trouver des donneurs appropriés. La procédure de transplantation comporte également des risques d’effets secondaires dangereux.
Plusieurs nouvelles méthodes de traitement de la drépanocytose sont actuellement en cours de développement. Ces méthodes impliquent l’édition de gènes des propres cellules de la moelle osseuse du patient pour produire de l’hémoglobine fonctionnant normalement. Ces méthodes de traitement évitent les risques associés aux greffes de moelle osseuse. Mais ces méthodes comportent également leurs propres risques car elles impliquent l’introduction d’un nouvel ADN et le clivage de brins d’ADN existants.
Une équipe de chercheurs, dirigée par le Dr David Liu du Broad Institute et le Dr Mitchell Weiss et le Dr Jonathan Yen du St. Jude Children’s Hospital aux États-Unis, a développé une méthode qui évite certains des risques d’autres approches d’édition de gènes. Cette méthode utilise une technique moléculaire appelée édition de base, qui modifie une seule lettre du génome sans couper aucun ADN.
Dans la drépanocytose, un T remplace un A à un endroit clé du gène HBB. Bien que l’édition de base ne puisse pas annuler ce changement, elle peut convertir le T en C à la place. Cette action produit une variante naturelle et non pathogène de l’hémoglobine appelée Hb-Makassar. Les chercheurs ont conçu un outil moléculaire appelé éditeur de base d’adénine, qui reconnaît la partie mutée du gène et convertit le T en C.
Les chercheurs ont utilisé l’éditeur de base d’adénine sur des cellules souches hématopoïétiques de patients humains atteints de drépanocytose. Jusqu’à 80 % des cellules avaient le gène de l’hémoglobine drépanocytaire converti en la variante de Makassar. Pour les tests, l’équipe a transplanté les cellules humaines modifiées dans un modèle murin de SCD. À 16 semaines après la transplantation, 68 % des cellules souches dérivées de donneurs avaient des gènes HBB modifiés en Hb-Makassar. Les globules rouges dérivés de ces cellules souches avaient considérablement réduit la falciformation.
Étant donné que les globules rouges humains ne peuvent pas survivre chez la souris assez longtemps pour des tests approfondis, l’équipe a ensuite prélevé des cellules souches d’un modèle SCD de souris, les a modifiées et a transplanté les cellules modifiées dans un autre ensemble de souris. Après 16 semaines, la variante Makassar représentait près de 80 % de l’hémoglobine des souris receveuses. Les souris témoins qui ont reçu des cellules non modifiées présentaient des symptômes de SCD caractéristiques : anémie, numération globulaire anormale, globules rouges en forme de faucille et une rate hypertrophiée. Les souris ayant reçu les cellules souches modifiées présentaient des symptômes considérablement améliorés.
Les chercheurs ont prélevé la moelle osseuse des souris qui avaient reçu les cellules souches modifiées et l’ont transplantée dans un nouvel ensemble de souris. Les nouveaux receveurs avaient une numération globulaire saine, confirmant la durabilité de l’édition des gènes. Les chercheurs ont en outre déterminé que la modification d’au moins 20 % des copies du gène SCD était suffisante pour maintenir des mesures sanguines saines. Ils n’ont détecté aucun effet secondaire chez les souris lors du processus d’édition de gènes.
« L’approche est prometteuse en tant que base d’un traitement ponctuel, ou peut-être même d’un remède ponctuel, pour la drépanocytose », explique Liu.
L’équipe travaille maintenant à développer davantage le concept, dans le but éventuel d’atteindre les patients.
.














:max_bytes(150000):strip_icc()/headache-576877516-599ca0730d327a0011b6bbcd.jpg)
:max_bytes(150000):strip_icc()/GettyImages-533768877-574b88775f9b58516549d5a1.jpg)
Discussion about this post